多肽及多肽合成简介
多肽和蛋白质是α-氨基酸以“肽链”(Fig. 1)连接在一起而形成的线型聚合物。 肽键是一个氨基酸的羧基与另一氨基酸的氨基发生缩合反应脱水成肽时,羧基和氨基形成的酰胺键。氨基酸是含有连接于α-碳原子的一个氨基(NH3)、一个羧基(COOH)、和一个可变侧链(R)的有机化合物。 通常,羧酸和羧基并不十分活泼,在酰胺键形成前需要活化羧酸(Fig. 2)。

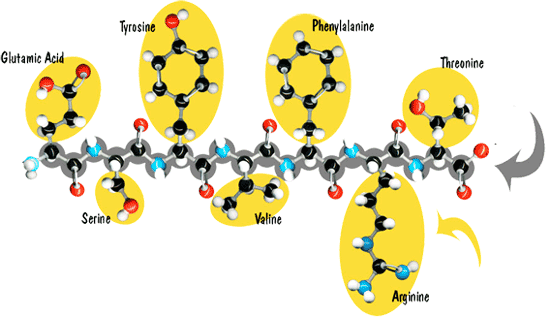
Fig. 1: 多肽结构
可控的 多肽合成 需要选择性地对各种功能基团进行保护和去保护:如氨基、羧基或侧链的官能团。侧链赋予了各个氨基酸不同的属性, 有助于指导蛋白的折叠。
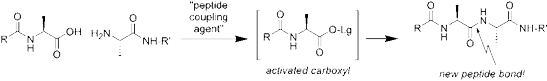
Fig. 2: 肽键经多肽偶联剂作用下耦合而成
有序的 多肽合成 需要对各种功能基团进行选择性的保护和脱保护: 包括氨基、羧基和侧链等功能基团。侧链基团赋予了每个氨基酸独特属性,并有助于决定蛋白的折叠。
目前,有两种多肽合成机制或策略。第一种是使用Fmoc基团保护氨基酸氨基端(对碱敏感, Fig. 3),第二种是使用Boc基团保护氨基酸氨基端(对酸敏感, Fig. 4)。
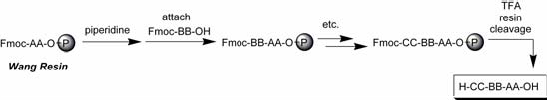
Fig. 3: Fmoc合成法 (Wang resin)
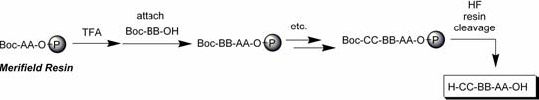
Fig. 4: Boc 合成法 (Merifield resin)
固相合成的合成顺序一般是从C端(羧基端)向 N端(氨基端)进行。固相多肽合成方法(SPPS)可以在每一个反应循环后通过洗脱的方法有效地去掉剩余的试剂以及可溶性的副产物,而合成的多肽仍被锚定在不溶的固相树脂上。树脂通常由聚苯乙烯组成。
多肽合成的有序进行和酰胺健的形成都需要使用氨基基团的可逆离子。三种常见的保护机制是: 叔丁基羰基(tBoc)、芴甲氧羰基(Fmoc)和N-Allyloxycarbonyl (Alloc)。
这些代表不同的保护和脱保护机制。当然,侧链功能基团也是需要进行保护和脱保护的。在第一个氨基酸锚定在树脂上后,它的氨基保护性基团Fmoc会被去掉。为了证实Fmoc已被去掉,可执行一项检测,即kaiser test。接着携带活化羧基的Fmoc-氨基酸会被加入(即耦合连接)。Fig. 5列出部分偶联剂例子。
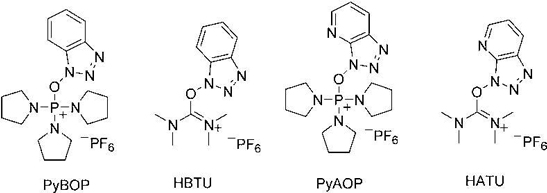
Fig. 5: 部分偶联剂
我们用kaiser test来检测耦合是否完全。这个过程在脱保护、耦合、洗脱循环中被反复执行,直到最后整条多肽被全部合成。接着合成的多肽被从树脂上裂解下来,同时侧链的保护基团也被去掉。多肽的纯化通常包括以下过程,先通过添加乙醚将多肽从裂解反应混合物中沉淀出来;接着将多肽和树脂混合物重悬在水或酸的水溶液中,通过过滤,去掉树脂。进一步纯化即凝胶过滤、离子交换层析和反相高效液相色谱法(reversed-phase HPLC)。
Fig. 6: 多肽形成
|